Un double anticorps développé au Tessin pour combattre le Covid et ses variants
Dans l'arsenal clinique de lutte contre le SARS-Cov-2, les vaccins occupent une place dominante. Mais de nouvelles perspectives thérapeutiques s'ouvrent aussi, comme les traitements à base d'anticorps monoclonaux, issus de la biotechnologie.
Deux fabricants américains proposent actuellement ces anticorps comme traitement curatif: Regeneron et son cocktail d'anticorps casirivimab et imbdevimab - un traitement rendu célèbre après avoir été administré à Donald Trump - ; et la firme Eli Lilly avec son bamlanivimab.
L'Allemagne a déjà commandé 200'000 doses du traitement Regeneron pour 400 millions d'euros. Soit 2000 euros pièce.
Efficace contre les mutants
Dans un laboratoire tessinois, on a peut-être trouvé une arme plus redoutable encore: une molécule à base d'anticorps baptisée Cov-X2. "On a testé le virus de la variante anglaise et l'anticorps fonctionne sans aucun problème, comme pour le virus standard. Les tests en laboratoire démontrent qu'il fonctionne également contre les variantes sud-africaine et brésilienne", assure le directeur du laboratoire de l'IRB à Bellinzone, Luca Varani, au 19h30 de la RTS.
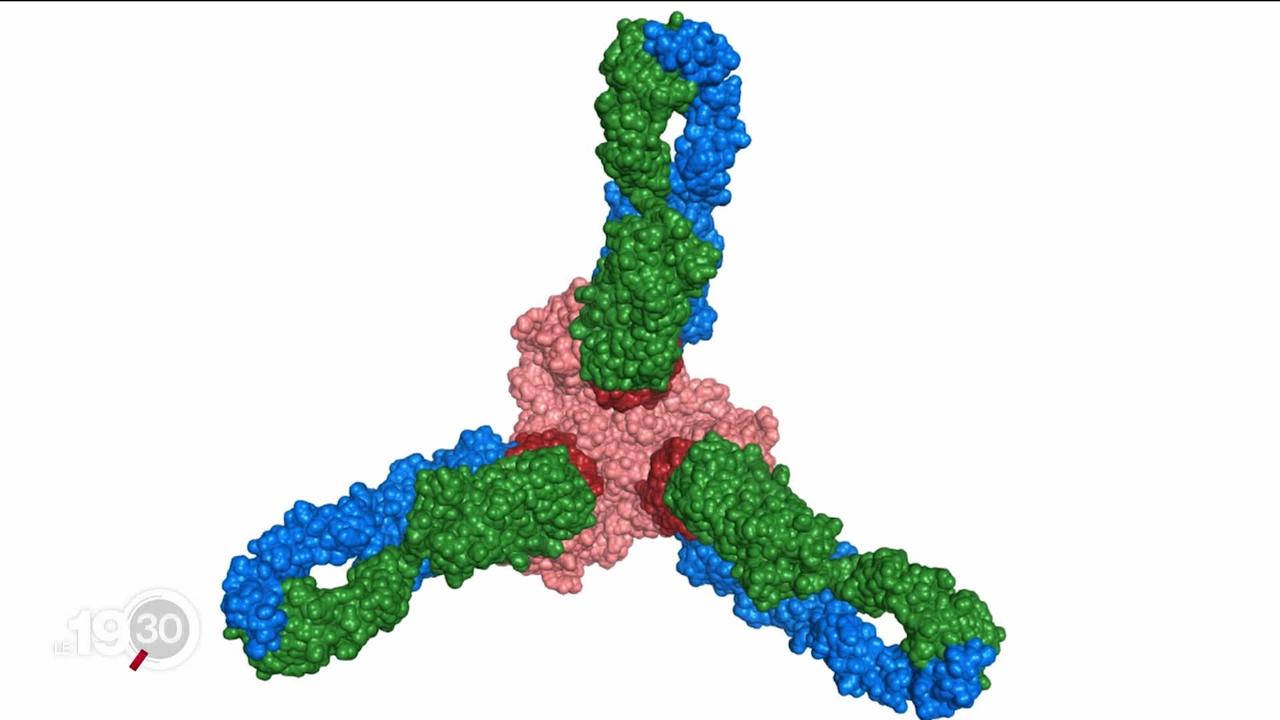
Contrairement aux anticorps d'Eli Lilly, la molécule est composée non pas d'un mais de deux anticorps prélevés chez des donneurs convalescents. Des bras colorés ci-dessous en vert et bleu s'attaquent au virus en rouge et l'empêchent de muter.
![Deux anticorps (en vert et bleu) s'attaquent au virus en rouge et l'empêchent de muter. [RTS] Deux anticorps (en vert et bleu) s'attaquent au virus en rouge et l'empêchent de muter. [RTS]](https://img.rts.ch/articles/2021/image/3q71iv-27713795.image?mw=1280)
Coopération
Les résultats (encore en "preprint") des tests précliniques menés sur des souris donnent de grands espoirs. D'après Nicolas Winssinger, professeur au Département chimie organique de l'Université de Genève, il s'agirait d'une véritable avancée: "Etant donné qu'il s'accroche au virus avec deux bras et tient la protéine du virus plus fortement, une mutation dans le virus aura un impact moindre que si l'anticorps n'avait travaillé qu'avec un bras", illustre l'expert. Autrement dit, la probabilité que l'efficacité de cet anticorps s'érode avec des mutations est moindre.
Le produit de Regeneron combine lui aussi deux anticorps monoclonaux, donc deux "bras", mais avec deux anticorps, tandis que la molécule développée par le laboratoire tessinois est concentrée dans une seule molécule. "Le bénéfice, lorsque les deux bras sont à proximité, c'est qu'ils coopèrent", précise Nicolas Winssinger.
Prévention et protection immédiate
Les anticorps monoclonaux offrent non seulement un espoir de traitement efficace, mais ils sont aussi un moyen de se protéger du virus. Leur coût très élevé en comparaison au vaccin ne permettrait toutefois pas d'en constituer une alternative. Pour Luca Varani, les deux produits doivent être complémentaires: "Il y aura toujours des personnes qui ne répondent pas bien à un vaccin, comme par exemple les patients cancéreux subissant une immunothérapie. Un anticorps les protégerait du virus".
Le directeur du laboratoire de l'IRB note aussi un deuxième atout de l'anticorps, il protège immédiatement, contrairement au vaccin, qui ne protège qu'après quelques semaines et une deuxième injection. "En cas d'infection virale dans une maison de retraite ou dans un hôpital, il n'est pas possible d'attendre plusieurs semaines pour qu'un vaccin fasse effet. L'administration d'anticorps aux individus non infectés, au contraire, les protégerait immédiatement."
Commande suisse chez Molecular Partners
Pour aller de l'avant, les chercheurs tessinois doivent désormais passer aux tests cliniques de phase I, soit sur 10 à 15 volontaires humains. "Cela nécessite des productions de grammes d'anticorps sous le contrôle de qualité le plus strict, conformément aux normes de sécurité internationales. Ce n'est pas une entreprise qu'un institut de recherche comme l’IRB peut mener seul", note Luca Varani.
Dans le meilleur des cas, les tests pourront débuter dans 4 à 6 mois à condition de trouver au moins 3 millions de francs. Jusqu'ici, l'IRB a reçu un financement du projet Horizon 2020 ATAC, mais rien de la Confédération.
En Suisse, l'Office fédéral de la santé publique (OFSP) à travers la voix de sa porte-parole Simone Buchmann dit avoir conclu un accord de réservation avec le laboratoire zurichois Molecular Partners (lire en encadré) pour un agent thérapeutique qui fait actuellement l'objet d'essais cliniques: "Le contrat donne au gouvernement suisse un accès prioritaire aux 200'000 premières doses et le droit de fournir jusqu'à 3 millions de doses supplémentaires", écrit-elle dans une réponse à la RTS.
Gabriel de Weck et Feriel Mestiri
Autre antiviral prometteur suisse
Le laboratoire de biotechnologie zurichois Molecular Partners développe lui aussi un traitement dont les résultats préliminaires s'annoncent prometteurs à la fois pour traiter et prévenir le Covid-19.
Son candidat antiviral ensovibep (MP0420) a débuté les essais cliniques de phase I à l'automne 2020. Les résultats sont attendus d'ici la fin du trimestre en cours.
Molecular Partners a reçu le soutien du groupe pharmaceutique Novartis, qui a réglé un versement initial de 20 millions de francs en liquide assorti d'une prise de participation de 6% à hauteur de 40 millions pour s'assurer les droits de développement avancés, de production et de commercialisation.
Selon les résultats d'une étude menée in vitro par le laboratoire de Spiez publiés en pré-print la semaine dernière, l'ensovibep a conservé "une efficacité et une activité très élevées sur tous les variants et mutants viraux testés".
Molecular Partners table aussi sur le lancement d'études cliniques de phases II, puis III au premier semestre et une potentielle autorisation d'utilisation d'urgence dans l'année.